Жесткость воды это
Жесткость воды что это такое
Проблемы водоподготовки в быту и на производстве решаются путем применения различных методик и специального оборудования. Ответ на вопрос, что такое жесткость в воде и как ее уменьшить до приемлемых величин - один из самых сложных и трудно решаемых даже при наличии доступных систем фильтрации. Вместе с тем высокое содержание растворимых солей негативно сказываются на состоянии здоровья человека, бытовых приборов и технологического оборудования.
Жесткость воды - это показатель качества, во многом определяющий ее физико-химические свойства и возможности применения. В предлагаемой статье рассматриваются причины этого явления, устанавливаются различия параметров жидкости в зависимости от концентрации солей. Также приводятся требования к жидкости и разбираются существующие бытовые и профессиональные методы ее умягчения.
Что такое жесткость воды
Оксид водорода (вода) - самая распространенная жидкость на земле, обладающая уникальными свойствами растворять в себе многие химические элементы и соединения. Понятие жесткости воды в определении трактуется как количественный показатель концентрации солей щелочноземельных и иных металлов. Преимущественно это соединения кальция и магния.
Термин общая жесткость воды возник в результате наблюдений за состоянием тканей после стирки. Особая структура материала, состоящего из отдельных нитей, способствует накоплению упомянутых солей металлов. При большом их содержании ткань, становится жесткой и грубой. Позже было замечено, что высокая концентрация таких соединений существенно снижает эффективность моющих средств.
Жесткость воды - это соли кальция и магния, образующие накипь на внутренних поверхностях нагревательных приборов и теплообменников. Это в свою очередь приводит к ухудшению эксплуатационных и экономических характеристик нагревательного оборудования. В отдельных случаях трубопроводы в буквальном смысле закупориваются, что делает невозможным их использование по назначению. Определить есть ли в воде жесткость можно даже в домашних условиях!
Основные причины образования жесткости воды
Фактически эта жидкость является универсальным растворителем, который при контакте с почвой и минералами насыщается содержащимися в ней веществами и химическими соединениями. Отвечая на вопрос о жесткости воды, и чем она обусловлена, необходимо выделить основные источники солей щелочноземельных металлов:
- Для подземных источников - это пласты известняка, сквозь которые просачивается жидкость.
- Для открытых водоемов и приповерхностных слоев - это геологические породы: природный гипс, доломит и другие.
- Ионы кальция и магния насыщают воду в результате химических реакции диоксида углерода и некоторых минералов.
- Микробиологические процессы в грунтах и на сельскохозяйственных угодьях в районах водосбора.
Помимо естественных причин повышенное содержание ионов жесткости в воды обусловлено также и техногенными. В составе стоков промышленных, строительных и коммунальных предприятий имеется большое количество примесей. В результате происходит вторичное загрязнение водоемов и водоносных слоев.
Естественные процессы химического выветривания горных пород и техногенные факторы определяют параметры жесткости воды питьевой или технической. Эти показатели неодинаковы для различных источников и постоянно изменяются:
- Повышаются в результате испарения влаги с открытых поверхностей водоемов.
- Снижаются при выпадении атмосферных осадков, таянии льдов и снега.
Значительное содержание извести в воде - это жесткость преимущественно естественного происхождения, характерная для подземных источников, в том числе и для артезианских скважин. Минерал вымывается из геологических пластов потоками жидкости при просачивании вглубь земной коры. Затем этот раствор через родники и ключи пополняет водный баланс открытых источников.
Происходит постоянный кругооборот, и жесткость воды в некоторой степени зависит от времени года. Весной в ходе таяния снегов и активных осадков он существенно уменьшается в другие периоды и, особенно при засухах - увеличивается.
Виды жесткости воды
Уровень содержания солей и их состав для разных источников водоснабжения как открытых, так и закрытых различаются и существенно. Возникает закономерный вопрос, а какова жесткость воды, и какой она может быть в зависимости от происхождения. Существует классификация по уровню насыщенности химическими веществами и соединениями, для удобства сведенная в таблицу:
Приведенная шкала наглядно показывает уровни жесткости воды, и в чем она измеряется в системах, принятых в разных государствах. Данная классификация отображает методические подходы к определению означенного показателя в соответствии с нормативными документами следующих стран:
- Россия. Государственный стандарт.
- Германия. Институт стандартизации - DIN.
- США. Агентства по охране окружающей среды Соединенных Штатов Америки - USERA.
Упомянутый градус жесткости воды - это единица измерения, принятая в западных странах. Этот показатель соответствует следующим значениям:
- В Германии (°dH). Одна часть CaO или 0,719 части MgO на 100 тыс. частей воды.
- В Британии (°e). 1 гран CaCO3 на один галлон жидкости.
- В США (ppm) и Франции (°TH). Одна часть CaCO3 на 100 тыс. частей воды.
При сравнительно невысоком уровне жесткости воды содержание ионов кальция в ней может достигать 70-80%, в тоже время насыщенность ионами магния редко превышает 50-60%. При увеличении уровня минерализации картина резко меняется: концентрация первых сильно уменьшается и редко доходит до 1 г/л; содержание же ионов магния часто превышает показатель 10 г/л. Такое соотношение особенно характерно для соленых озер, не имеющих стока.
Классификация вод осуществляется не только по уровню жесткости, но и с учетом ее гидрохимического состава. По данному признаку различают следующие разновидности:
- Общая.
- Временная (карбонатная).
- Постоянная (не карбонатная).
Для каждого типа характерно определенное соотношение содержания солей кальция, магния и других. Соответственно методы уменьшения жесткости воды зависят от ее вида, и состав оборудования для конкретного случая определяется с учетом реальных показателей. Рассмотрим этот вопрос подробнее.
Общая жесткость воды
Исследуемый показатель в значительной мере зависит от гидрохимического состава жидкости и уровня насыщения солями кальция и магния. Общая жесткость - это свойство воды, определяемое суммарным содержанием гидрокарбонатов и других соединений названных элементов. Данная характеристика имеет две составляющие:
- Карбонатная (временная). Связана с наличием в жидкости гидрокарбонатов кальция (Ca2+) и магния (Mg2+), которые при нагревании и кипячении образуют CaCO3 и Mg(OH)2 с выделением углекислого газа (CO2).
- Некарбонатная (постоянная). Определяется присутствием фосфатов, хлоридов, сульфатов, силикатов и нитратов этих щелочноземельных металлов.
Перечисленные соли, определяющие общую жесткость воды, при кипячении не разлагаются и их удаление из жидкости требует иных методов. Для численного выражения этого показателя используют специальную физическую единицу 1 ммоль-экв./л, которая соответствует содержанию 20,04 мг/л катионов кальция либо 12,16 мг/л катионов магния.
Общая жесткость подземных вод (в некоторых регионах), а также морских и океанских может достигать 80 и даже 100 ммоль-экв/л, что делает их непригодными для использования. В тоже время в реках и озерах, находящихся в таежных районах данный показатель находится на уровне от 0,1 до 0,2 ммоль-экв/л. Такой водой практически невозможно смыть мыльный раствор.
Временная жесткость (карбонатная)
Природная вода содержит значительное количество катионов щелочноземельных металлов. Временная (магниевая и кальциевая) жесткость воды - это показатель присутствия в жидкости гидрокарбонатов названных химических элементов. При нагревании растворимость этих соединений (при уровне pH превышающем 8,3 единицы) существенно уменьшается, и они переходят в следующие формы:
- осадок хлопьевидный;
- беловатая пленка на поверхности;
- кристаллическая накипь.
Временная жесткость воды по кальцию и магнию при этом полностью устраняется - отсюда собственно и название. Помимо кипячения уменьшить означенный показатель возможно используя ионообменные методы и технологии обратного осмоса.
Постоянная жесткость (некарбонатная) воды
Помимо гидрокарбонатов кальция и магния в источниках водоснабжения присутствуют в значительных количествах соли азотной, серной и соляной кислоты. Под некарбонатной жесткостью воды подразумевается суммарное содержание этих химических соединений. Последние при нагревании остаются в растворенном состоянии и не выпадают в осадок.
Некарбонатная жесткость воды именно поэтому и называется постоянной, а для ее устранения необходимо специальное оборудование. Существенно уменьшить концентрацию этих растворимых соединений возможно при использовании ионообменных технологий и деминерализации. Особенно высока эффективность у современных систем умягчения.
Действующие нормативы жесткости воды
Нормы жесткости, характеризующие качество источников водоснабжения, регламентируются во всех развитых странах. В Российской Федерации принят ГОСТ 31954-2012, которым устанавливаются предельные значения общей жесткости воды и определяются способы ее вычисления. Этим документов утверждены два метода: комплексонометрический - основной и атомной спектрометрии - арбитражный.
Жесткость общая воды в части гигиенических норм устанавливается требованиями СанПиН 2.1.4.1075-01, утвержденным Постановление от 26.09.2001 года. Суммарный показатель содержания солей щелочноземельных металлов не должен превышать предельно-допустимых концентраций, которые определены в размере 7,0 и 10,0 мг-экв./л. Второе значение может быть установлено только по решению главного санитарного врача с учетом используемой технологии водоподготовки для конкретного населенного пункта.
Расчет жесткости воды
При определении общей жесткости воды допускается применение вычислительных методов. Этот показатель измеряется в ммоль/дм3 или моль/м3 и описывается следующей формулой:
ЖО = [Ca2+] + [Mg2+] = ЖК + ЖНК;
Данное уравнение позволяет вычислить среднюю жесткость воды, в ней приняты следующие обозначения:
ЖО - общая.
ЖК - карбонатная (временная).
ЖНК - некарбонатная (постоянная).
Для того чтобы рассчитать общую жесткость воды необходимо знать молярную масса катионов кальция и магния, а также анионов сернистой кислоты. Результаты вычислений могут быть использованы для определения наиболее подходящего метода ее очистки. Подобные расчеты проводятся специалистами профильных лабораторий на основании опытных данных.
Методы определения уровня жесткости воды
Как определить жесткость воды? Точная оценка количественных параметров содержания солей производится специализированными лабораториями. В соответствии с ГОСТ 31954-2012 общая жесткость воды определяется комплексонометрическим методом в такой последовательности:
- Проба разделяется на две равные части.
- В химическую колбу наливают 100 мл исследуемой воды, добавляют к нему 5 мл буферного раствора и сухой индикаторной смеси в количестве 0,06-0,10 г. Получившийся состав титруется трилоном Б.
- Аналогичные действия выполняются в отношении второй части пробы в другой лабораторной посуде. Добавление трилона Б осуществляется в два приема: сначала - на 0,5 см3 меньше, чем при исследовании первого образца. После тщательного перемешивания вводится остаток.
Обработка результатов, полученных с использованием описанного метода определения общей жесткости воды, выполняется по следующей формуле:
Ж = M•K•Vтp/Vnp,
где M - коэффициент пересчета;
K - коэффициент поправочный;
Vтp - объем трилона Б, использованного для титрования;
Vnp - количество исследуемой воды из пробы.
Результат испытаний согласно данному методу определения общей жесткости в питьевой воде, а также технической, вычисляется как среднеарифметическое от двух полученных значений. Это позволяет минимизировать погрешность расчетов.
Бытовые способы умягчения воды
Высокая соленость и жесткость воды, используемой в пищу и в хозяйственно-бытовых целях, может принести вред здоровью и привести к выходу из строя бытовой техники. В домашних условиях уменьшить этот показатель можно путем термической и химической обработки исходной жидкости.
Устранимая жесткость воды - карбонатная (временная) снижается при длительном кипячении. В процессе нагрева гидрокарбонатные соединения кальция и магния распадаются и переходят в твердое состояние. Они образуют накипь на стенках посуды, хлопьевидный осадок и поверхностный налет. Последние легко удаляются фильтрованием или отстаиванием.
Химическая обработка в целях снижения жесткости исходной воды выполняется при помощи извести и соды. Первый реагент обеспечивает умягчение жидкости с незначительным содержанием некарбонатных и высокой насыщенностью карбонатными соединениями. Для повышения эффективности данного метода дополнительно применяются реагенты коагулянты.
Комбинирование извести и пищевой соды позволяет уменьшить общую жесткость речной или колодезной воды до значений 1,4-1,8 мг экв./л. Химическая обработка обеспечивает улучшение качества жидкости по данному показателю, но требует очень точной дозировки реагентов. Кроме того она непригодна для приготовления пищи и питья.
Профессиональные методы снижения жесткости воды
Качественное умягчение исходной воды до требуемого уровня возможно только при использовании специального оборудования - фильтров от жесткости воды. Довести показатели жесткости до соответствия требованиям упомянутого СанПиН и "ГОСТ вода питьевая" позволяют следующие технические устройства:
- Фильтры умягчения.
- Ионообменные фильтры.
- Системы обратного осмоса.
При выборе установки для снижения жесткости воды, прибором для ее определения устанавливают точный гидрохимический состав и количественное содержание солей. Оборудование подбирается по результатам испытаний и с учетом требований заказчика к качеству обработанной воды.
Фильтры умягчения
Процесс уменьшения общей жесткости воды должен быть достаточно эффективным и недорогим. В настоящее время основным способом умягчения является метод натрий-катионирования (фильтры умягчения), который применяется и в быту, и в промышленных масштабах. Поток воды пропускается через ионообменные колонны, где происходит замещение кальция и магния катионами натрия. На поверхности полимерных смол происходят следующие химические реакции:
Ca2+ + 2RNa = 2Na+ + R2Ca
Mg2+ + 2RNa = 2Na+ + R2Mg
В результате общая жесткость доводится до уровня питьевой воды по ГОСТу, что делает возможным ее применение для приготовления пищи и хозяйственно-бытовых нужд.
Такие фильтрующие колонны применяются в составе многоступенчатых систем, в которых вода сначала очищается от механических примесей и железа. Это позволяет повысить ресурс основных картриджей, который естественным образом уменьшается в процессе расходования ионов натрия и накопления ионов жесткости. Для восстановления свойств ионообменных смол в системе предусмотрены баки с раствором поваренной соли, клапаны и блоки управления.
Когда датчик фиксирует повышение жесткости воды в ppm, подача ее перекрывается и производится обратная промывка содержимого колонны солевым раствором. После восстановления характеристик полимерных гранул, подача реагента прекращается. Открывается клапан и возобновляется процесс умягчения.
Управление работой такого фильтра, обеспечивающего уменьшение общей жесткости природной воды, в зависимости от комплектности осуществляется в автоматическом или в ручном режиме. В первом варианте используются электронные датчики и электроклапаны. Во втором случае переключение установки в режим регенерации выполняется человеком по истечении определенного периода времени.
Ионообменные фильтры
Данный метод умягчения по принципу действия в значительной мере аналогичен описанному выше. Замещение ионов, обуславливающих жесткость воды, в них происходит с помощью многокомпонентных смол типа Ecomix или Ecotar. В состав этих фильтрующих загрузок входят следующие материалы:
- Смола инертная обеспечивает обезжелезивание воды.
- FerroSorb удаляет соединения железа и марганца.
- HumiSorb нейтрализация органических примесей.
- Смола ионообменная для умягчения воды.
- Песок кварцевый в виде подложки, обеспечивающей равномерное распределение потоков жидкости.
Применение многокомпонентных составов для фильтрующих установок позволяет снизить общую жесткость воды за счет реакции замещения катионов кальция и магния. Данная технология более универсальна в сравнении с фильтрами умягчения, однако и менее эффективна. При этом финансовые затраты на ее приобретение и содержание выше нежели у специализированных элементов.
Обратный осмос
Использование полупроницаемых мембран обеспечивает высочайший уровень очистки жидкости от всех видов примесей. В современных системах обратного осмоса показатели общей жесткости воды после кондиционирования на мембранах типа DRO-4040 или DRO-8040 снижаются более чем на порядок. Такие установки применяются для опреснения соленых воды (океанских, морских, озерных и подземных).
Мембраны имеют пористую структур, пропускающую только молекулы воды и задерживающую соединения кальция и магния (гидрокарбонатные и соли кислот). В результате происходит снижение общей жесткости воды до значений, делающих возможным ее применение в фармацевтике и микроэлектронике. Пермеат практически не содержит микроэлементов и нуждается в минерализации для питья и приготовления пищи.
Такие показатели, существенно превосходящие ГОСТ для питьевой воды по общей жесткости, явно избыточны. С учетом высоких начальных затрат на приобретение, монтаж и последующее обслуживание использовать установки обратного осмоса в быту экономически невыгодно. Гораздо эффективнее для таких целей применять традиционные фильтры умягчения.
Что такое общая жесткость воды
Получив представление о жесткости воды, и как она влияет на организм, а также на бытовую технику и другое оборудование, приходим к выводу о необходимости ее нормализации. Кустарные методы (кипячение или химобработка) не обеспечивают надлежащего качества воды. Кардинальное решение проблемы возможно только при использовании современных фильтрационных установок.
Компания Diasel Enginereeng предлагает высокоэффективные системы водоподготовки: фильтры умягчения и ионообменные, а также обратноосмотические. Мы предоставляем полный комплекс услуг по проектированию установок, подбору, монтажу и запуску оборудования. Наши специалисты обеспечивают их сервисное и гарантийное обслуживание. Перейти в раздел "Контакты".
что это такое, как определить вид общей жесткости и в чем она измеряется, таблица определения норм в единицах измерения, какой вред человеку наносит и как устранить
Сегодня мы расскажем о понятии «жесткость воды», что это такое, ее виды, в каких единицах измерения ее определяют, есть ли допустимые нормы для питья, а также чем она плоха и какой вред для человека она может нанести. С данным термином мы сталкиваемся практически ежедневно при просмотре рекламы, а также при использовании порошка или моющего средства для посудомоечной машины, при установке фильтра. Но зачастую мы не подозреваем, какой показатель именно у нас – общий по городу или индивидуальный.
Вторая распространенная проблема, когда сталкиваются с данной характеристикой, – при монтаже собственной, индивидуальной точки доступа к скважине или колодцу. Обычно требуется произвести химический анализ, чтобы определить, какая фильтрационная система необходима. И при высоком содержании примесей (кальция и магния) требуется специальное оборудование для устранения данных солей. Но если вам не подскажет это специалист, необходимо самостоятельно разобраться в теме. Давайте это и сделаем.
Жесткость воды – что это такое
Это совокупное физико-химическое свойство жидкости, которое предопределяет ее использование и возможности эксплуатации в различных условиях, питьевое качество. Согласно второму определению, это уровень содержания в водном растворе примесей – солей щелочноземельных металлов (они в мельчайших фракциях находятся в подземных слоях), магния, кальция, а также других элементов, которые полностью не растворяются. Для этого следует понять, что Н2О – это только в учебниках химии, а в жизни химический состав гораздо более разнообразен.
Как понять, что вода жесткая, и что это значит? Легко определить повышенную жесткость можно в домашних условиях обычным кипячением. Если по краям после такого теста остался белый след, который красится как меловая крошка, то, скорее всего, это кальциевые отложения.
Данное свойство очень важно с точки зрения хозяйственного значения и потребительских качеств. Особенно это значимо с двух сторон:
-
для здоровья потребителей при употреблении в качестве напитка, а также при использовании в гигиенических процедурах, ведь волосы после мытья такой водой могут стать безжизненными и сухими, а кожа грубой;
-
для долговечности работы нагревательных элементов в стиральной и посудомоечной машинах (ТЭНы), чайниках и иных нагревателях – на них образуется накипь и они быстро выходят из строя.
Также это оказывает негативное воздействие на качество стирки, поскольку химические элементы препятствуют протеканию нормальной реакции стирального порошка, он может слабо вспениваться или недостаточно хорошо проникать в структуру ткани и избавлять ее от загрязнений.
Окружающая природа, горные породы и залежи различных полезных минералов совершенно разные на каждом участке гидродобычи (это зависит от почвы, близлежащих предприятий, глубины пролегания источника), поэтому в разных водоемах и жесткость различная. Именно по этой причине перед использованием обязательно берут пробы, делают химический анализ образца на наличие вредных веществ. Угадать наверняка без этого очень сложно, но можно указать на такую закономерность – чем глубже пролегают грунтовые воды, тем они более жесткие, на поверхности они мягче, поскольку протекают через меньшее количество различных земельных слоев.
Вторая тенденция характерна для природных, естественных водоемов и связана с таянием снегов и дождями. Максимальный показатель зимой, а минимальный – весной сразу после схода льда.
Дадим еще один простой вариант определения, каких примесей больше – магния или кальция. Магниевые соли хуже растворяются, поэтому дают осадок, также они имеют горький привкус.
А теперь посмотрим на сравнительную таблицу:
| Градусы dH |
| Жесткость в мг. х экв/л | Аналог в ppm | ||
| 13 – 22 | Жесткая | 8 – 12 | 210 – 320 | ||
| 9 – 12 | Средняя | 4 – 8 | 140 – 210 | ||
| 5 – 8 | Мягкая | 1,4 – 4 | 70 – 140 |
Шкала жесткости воды или как определить параметр по таблице
Сперва дадим график, согласно которому любую жидкость можно разделить на классы:
Alkaline – щелочная, она же карбонатная. Степень определяется наличием и концентрацией карбонатов и гидрокарбонатов кальция и магния. Особенность в том, что данные микроэлементы выпадают в осадок сразу после кипячения, поэтому такие водные растворы также называют непостоянными или временными.
Вторая часть шкалы Acidic – то есть, кислотосодержащая или некарбонатная. В ее составе не карбонаты и гидрокарбонаты, а кислотные соли на основе вышеперечисленных химических веществ. И они более устойчивые.
И есть также общая – она включает суммарное количество примесей. Чаще всего в бытовых ситуациях определяется именно последняя, то есть итоговая сумма микроэлементов. Но в ряде ситуаций имеет наибольшее значение именно одно состояние магниевых и кальциевых солей, их соединения. Если в анализе жидкости или в иной ситуации вы видите такую шкалу, то можно ориентироваться по цветам и картинке выше. То есть от 0 до 7 вы имеете дело с кислотными солями, а с 7 до 14 – с гидрокарбонатами.
Единицы измерения
Мы объяснили, какую воду называют жесткой, чем обусловлена общая жесткость и какие виды различают, теперь обсудим, в чем измеряется показатель и что на него влияет.
К сожалению, нет мирового стандарта, поэтому, используя аппаратуру европейского изготовления, будьте готовы к непонятным на первый взгляд обозначениям. Российскими учеными были установлены следующие единицы – моль на кубический метр. А перед этим ставится число, которое соответствует значению перевоплощения в миллиграммы на литр. А что можно встретить еще:
-
d° или dH – придумали в Германии, но применяют на всей территории Запада;
-
f° – пишут во Франции;
-
ppm CaCO3 – используют в США.
Жесткость: виды
По количеству примесей можно разделить воду на:
-
Мягкую. Она соответствует небольшой доли микроэлементов в составе. Получить ее можно после многочисленной обработки – специальной фильтрации, перегонки или многоразового кипячения, когда из-за термального воздействия карбонаты выпадают в осадок. Наибольшая мягкость у дождевой воды. Стоит отметить, что она благотворно воздействует на кожу, волосы, а также на здоровье в целом.
-
Среднюю. Это самый распространенный вариант, который считается приемлемым для бытовых и промышленных нужд. Именно поэтому такого качества жидкость идет по городскому и, вероятнее всего, по частному трубопроводу. Она вполне пригодна для приготовления пищи. В большинстве открытых природных водоемов вода тоже преимущественно средней жесткости.
-
Жесткую. В ней либо искусственным путем растворяют примеси, либо влага проходит через такие слои почвы, что сама быстро приобретает высокую концентрацию веществ. Самым распространенным вариантом можно считать морскую воду.
Как измерить и понять, допустимая или повышенная жесткость – способы
Представляем три варианта:
-
Наиболее точный – заказать лабораторный анализ. Во время пристального изучения будет произведен разбор на химические вещества, поэтому справка не только покажет общий показатель, но и конкретное содержание микроэлементов – какие и в каком объеме присутствуют в образце. Необходимо делать такую экспертизу владельцам частных домов при оборудовании скважины или колодца и заказе фильтрационной системы.
-
Быстрый и доступный каждому. Для этого стоит приобрести тестер в виде бумажной полоски. Его нужно опустить в жидкость, подождать указанный период, а затем определить цвет индикатора. Дело в том, что на активную части нанесен реагент, который вступает в реакцию и показывает количество примесей. Минус в сложности интерпретации и достаточно неточных результатах.

-
Домашний химический опыт. В два одинаковых мерных стакана следует нарезать по одному грамму хозяйственного мыла 72%. Затем залейте их подогретой водой – в одну емкость дистиллированной, во вторую водопроводной. В первом бокале будет уровень 7 см. А во втором – остановитесь вливать жидкость в тот момент, когда появится мыльная пена. Затем измерьте разницу влитой влаги. Каждый 1 см раствора соответствует двум °dH.
Какая должна быть оптимальная жесткость воды – норма
Как и единиц измерения, так и стандартов для всего мира общих нет. Зато в России в 2014 году появились жесткие нормативы, закрепленные ГОСТ 31865-2012. В нормативном документе показатель указывается в градусах и обозначается как °Ж. Он соответствует одному мг-экв/л. Посмотрим на таблицу нормативов, принятых у нас и в Америке:
| Качество жидкости |
| Пределы в США, в мг-экв/л | ||
| Мягкая (Soft) | <2 | <1,2 | ||
| Средняя (Moderate hardness) | От 2 до 10 | От 1,2 до 2,4 | ||
| Жесткая (Hard hardness) | >10 | От 2,4 до 3,6 | ||
| Очень жесткая (Very Hard hardness) | Нет нормы | >3,6 |
Как видим, российские требования гораздо более мягкие. Именно по этой причине бытовая техника, произведенная в Америке, служит гораздо меньше в контакте с нашим трубопроводом, чем у себя на родине.
Сравнивая европейские показатели, на примере Германии, мы сталкиваемся с такой же проблемой – у нас слишком гибкие рамки среднего качества. Таким образом, фактически любая водопроводная вода подходит под норматив.
Но употреблять такую жидкость попросту небезопасно, поэтому не стоит надеяться на государственные нормы, берегите здоровье своих домочадцев самостоятельно. Для этого устанавливайте системы фильтрации – обратитесь в компанию «Вода Отечества» для комплексной услуги установки фильтрационной системы на вашем участке.
Нормы для питьевой воды
Данный показатель регулирует не столько ГОСТ, сколько Всемирная Организация Здравоохранения и СанПиН. По рекомендации ВОЗ в одном литре жидкости для питья не может быть растворено более 30 мг магния и 80 мг кальция. А СанПиН 2.1.4.1074-01 предопределяет до 50 мг на магниевые отложение, кальциевые соли не регламентируются. Зато указана общая жесткость – до 7 градусов.
Влияние жесткой и мягкой воды – как отличить, рекомендации
ВОЗ утверждает, что употреблять необходимо только жидкость низкой или средней жесткости с установленными границами для примесей. Не всегда водопроводный ресурс, к сожалению, соответствует этим нормативам. Негативные последствия использования воды с повышенной жесткостью приводят к:
-
скорым поломкам бытовой техники – часто приходится заменять нагревательный элемент;
-
неисправностям инженерных систем – стенки труб постепенно разрушаются из-за образования отложений, а также засоряются;
-
испорченному здоровью;
-
мелким неприятностям – например, меняется вкус еды или качество постиранных вещей (моющий состав хуже пенится), мягкость вымытых волос.
Рекомендуем не дожидаться негативного воздействия и установить мощную систему фильтрации. Также стоит использовать не водопроводную, а специально подготовленную для питья жидкость, а при стирке или во время запуска посудомоечной машины добавлять специальные средства от накипи.
Вред для человека
Если соли поступают в чрезмерном количестве, они не успевают выводиться естественным образом и скапливаются в мочевых протоках и пузыре, почках – так начинается мочекаменная болезнь.
При умывании кожа становится более сухой, может образоваться раздражение. А на волосах появляется корочка, которая препятствует их естественному увлажнению и питанию подкожным жиром. Они становятся безжизненными.
Мясо, приготовленное в водном растворе с большим содержанием кальция, хуже усваивается организмом.
Как избавиться от жесткости воды и от чего она зависит
Если перед вами стоит вопрос что делать непосредственно с водопроводной жесткой водой, то выходов из ситуации не много:
-
поставить фильтр внутри квартиры, регулярно проверять систему и менять кассеты;
-
кипячение – стоит учесть, что данным способом можно убрать только карбонатный осадок, он останется внизу чайника или на его стенках, но если примесь в виде магниевых и кальциевых солей, способ не подходит;
-
заморозка – емкость следует проморозить так, чтобы на 90% образовался лед, а остальные 10% – слить, ведь именно концентрированный раствор замораживается медленнее всего.
Как повысить и понизить жесткость в аквариуме
Аквариумные рыбки – очень прихотливые создания, даже морские виды. У них всегда есть пределы, родной ареал обитания. Если вы хотите, чтобы они жили и размножались, следует воссоздать все необходимые условия.
Если нужно увеличить показатель солей, на дно можно положить известняк или мрамор, добавить хлористый кальций или магнезию.
В обратном случае придется прибегнуть к одному из вышеперечисленных трех способов. Чем больше объем резервуара, тем выгоднее будет создание фильтрационной системы.
Как избавиться от примесей в скважине
При бурении индивидуальной точки доступа к ресурсу просто необходимо делать предварительный анализ. Очень часто от этого зависит выбор расположения, а также глубина пролегания труб и насоса. Но если на участке испорченные грунтовые воды, поскольку они протекают через многочисленные солесодержащие почвенные слои, то и выбор места особенно не поможет, нужно производить фильтрацию. Обратитесь в компанию «Вода Отечества», чтобы специалисты выбрали для вас индивидуальное комплексное решение.
Методы устранения жесткости
Их несколько, все – эффективные. Выбирать следует, ориентируясь на конкретные показатели и степень эксплуатации – постоянно или сезонно.
Термоумягчение
Иными словами, это обычное кипячение. Следует немного приоткрыть крышку и ждать полного осадка примесей. Но если концентрация превышает 4 мл на литр, то способ не эффективен, поскольку испарение влаги произойдет быстрее, чем полное осаждение частиц.
Реагентное умягчение
В качестве реагентов чаще всего выступает обычная пищевая сода и известь. Они поочередно вводятся в раствор, отдельные химические элементы вступают с ними в реакцию с высвобождением Н2О и выпадают в осадок.
Катионирование
Это обессоливание с использованием катионов натрия или водорода. В первом случае это добавление обычной поваренной соли – что недорого, а также просто в утилизации продуктов регенерации.
Обратный осмос
В качестве фильтра выступает мембрана из ацетилцеллюлозы. С ее помощью достигается практически дистиллированная чистота. Такие установки небольшие, они хорошо берегут энергию. Но есть и минус – из раствора убираются практически все микроэлементы, а они важны для жизнедеятельности.
Электродиализ
Экологичный способ обессоливания. Он основывается на том, что вещества (положительные и отрицательные ионы) притягиваются к электродам под воздействием электрического заряда.
Дистилляция
Это промышленная перегонка жидкости. В ходе нагрева образуется водяной пар. Он впоследствии охлаждается и собирается как конденсат.
Вместо заключения
Мы рассказали, от чего зависит жесткость воды, чем она опасна и как ее устранить. Завершая тему, посмотрим видео:
Что такое жесткость воды: уровень и методы определения
Жесткость – параметр качества воды
Жесткость питьевой воды – одна из качественных характеристик воды, которое обуславливается наличием в воде солей двух щелочноземельных металлов - кальция и магния. Жесткость имеет значение для оценки качества любой используемой воды, технической, питьевой и воды, используемой для нужд промышленных предприятий с заданными характеристиками.
Наибольшее влияние на уровень жесткости воды оказывает количество катионов кальция, несколько в меньшей степени – магния. Катионы стронция, железа и марганца также оказывают влияние на жесткость воды, однако их вклад в общую жесткость воды так мало, что на практике обычно пренебрегают их значениями.
Общая жесткость определяется суммой временной и постоянной жесткостью воды.
Постоянная жесткость воды – кальциевые и магниевые соли соляной, серной, азотной кислот, т.е. сильных кислот. Такие соли жесткости в воде при кипячении не выпадают в осадок и не кристаллизуются в виде накипи.
Временная жесткость воды – показатель, наличия в воде карбонатов и гидрокарбонатов кальция и магния, которые при кипячении и показателях рН больше 8,3, практически полностью выпадают в хлопьевидный осадок, кристаллизуются в виде накипи или образуют пленку на поверхности воды.
Как соли кальция и магния попадают в природную воду, ведь вода, выпадающая в виде осадков, как и талая вода, не содержат солей?
Это происходит следующим образом: вода, напитывается солями, содержащимися в известняках, гипсах и доломитах залегающих в толщах земли.
Это основной источник этих солей. Кроме этого, выветривание горных пород, также может оказывать влияние на карбонатную жесткости воды.
Согласно методам определения жесткости воды по гидрохимии считается:
- 0-4 мг-экв./л – мягкая вода
- 4-8 мг-экв./л – средней жесткости
- 8-12 мг-экв./л – жесткая вода
- Больше 12 мг-экв./л – очень жесткая
Это касается оценки общей минерализации воды, но для питьевой воды российский СанПиН определяет предельно допустимые концентрации 0-7 мг-экв/л.
Специалисты в области фильтрации условно делят жесткость питьевой воды так:
- 0-1,5 мг-экв/л – мягкая вода
- 1,5-2 мг-экв/л – оптимальная питьевая вода
- 2-5 мг-экв/л – жесткая вода
- 5-7 мг-экв/л – сверхжесткая вода
- Больше 7 мг-экв./л – не питьевая вода, за пределами рекомендованных значений.
Можно разделить природную воду на поверхностную и подземную.
Поверхностная вода обычно имеет меньшую жесткость, поскольку она разбавляется в значительной степени осадками и талыми водами. Этим объясняется и факт сезонных изменений показателей общей жесткости для поверхностных вод.
Состав подземных вод более постоянен, и обычно имеет большие значения, чем у поверхностной воды, по общей жесткости.
Питьевая вода должна иметь оптимальный состав по количеству солей жесткости.
Слишком много солей – риск возникновения мочекаменной болезни, заболеваний костей, суставов. Слишком мало солей – соли вымываются из организма, кости приобретают большую ломкость, возрастает риск заболеваний суставов, сосудов.
По мнению некоторых исследователей, в регионах с пониженным уровнем жесткости воды, также возрастает риск сердечнососудистых заболеваний. Это подтверждается статистикой по странам Европы и Северной Америке, исследованиям в российских регионах с разными средними показателями по жесткости воды.
Также жесткая вода образует накипь, что приводит к уменьшению сроков службы бытовой технике, преждевременному износу водонагревательного оборудования, портит сантехническое оборудование.
Вода, уровень жесткости которой меньше двух мг-экв/л способна сильнее, чем более жесткая вода оказывать на водопроводные трубы коррозийное воздействие, поскольку имеет более низкую щелочность.
Поэтому, в ряде случаев, особенно в теплоэнергетике, иногда приходится проводить дозирование карбонатной жесткости воды с целью достижения оптимального соотношения между коррозионной активностью воды, ее водородному показателю и содержанию кальция и магния.
В настоящее время ряд специалистов, ссылающиеся на данные ВОЗ, утверждают, что имеющаяся статистика не позволяет однозначно считать мягкую и жесткую воду опасной для здоровья человека. И все же имеющиеся данные подтверждают зависимость водно-солевого баланса в организме человека от этих факторов, а отсутствие нормативной доказательной базы на уровне Всемирной Организации Здравоохранения, не причина закрывать глаза на качество питьевой воды по количественным показателям солей жесткости - солей кальция и магния.
Закажите консультацию специалиста компании Гейзер
Остались вопросы? Мы всегда готовы предоставить консультацию по всем вопросам очистки воды!
Жесткость воды что это такое
Жесткость воды — совокупность химических и физических свойств воды, связанных с содержанием в ней растворенных солей щелочноземельных металлов, главным образом, кальция и магния (так называемых «солей жесткости»). Вода – сложное природное вещество, в состав которого входит целый набор микроэлементов. В том или ином виде вода содержится во всех живых организмах. Что подразумевается под понятием жесткость, и что определяет данный показатель?
Подробнее про жесткость воды
Жесткость – это свойство воды, которое определяет ее потребительские качества и имеет важное хозяйственное значение. В процессе кипячения жесткая жидкость образует накипь на стенках и внутренних деталях нагревательных приборов, что вызывает ухудшение теплотехнических характеристик бытовой техники. Не особенно подходит она и для стирки, поскольку способствует снижению очищающих характеристик моющих средств и увеличивает их расход.
| Градусы dH | Характер воды | Жесткость в мг. х экв/л. | Эквивалент в mg/L |
| 23 — 34° | Очень жесткая | выше 12 мг х экв/л | 320 — 530 ppm |
| 13 — 22° | Жесткая | 8 – 12 мг х экв/л | 210 — 320 ppm |
| 9 — 12° | Средней жесткости | 4 – 8 мг х экв/л | 140 — 210 ppm |
| 5 — 8° | Мягкая | 1,5 – 4 мг х экв/л | 70 — 140 ppm |
| 0 — 4° | Очень мягкая | До 1,5 мг х экв/л | 0 — 70 ppm |
Откуда берется высокая жесткость? Ее определяет наличие солей магния и кальция – химических компонентов, выполняющих роль активных регуляторов различных химических процессов в окружающей среде. Естественно, что жидкость, которая берется из разных водоемов, может иметь ту или иную степень жесткости. При этом река, озеро и любой другой источник пополняются из подземных источников, протекающих в известняковых пластах. Проходя через них, вода обогащается солями жесткости, а значит, будет жесткой. Для сравнения – данный показатель у поверхностных вод всегда заметно ниже, чем у подземных. Жесткость воды в природных источниках постоянно изменяется. Максимальных отметок она достигает зимой, а минимальных – весной, во время таяния снегов.
Таким образом, жесткой является та вода, которая содержит соли магния и кальция в больших количествах. Кстати, магниевые соли растворяются хуже кальциевых, и жидкость с их высоким содержанием имеет выраженный горький вкус.
Шкала жесткости воды
Выделяются следующие виды жесткости:
- Общая – определяется как суммарная концентрация ионов магния и кальция.
- Карбонатная – зависит от наличия в воде карбонатов, гидрокарбонатов кальция и магния. Практически полностью устраняется в ходе кипячения, поэтому второе название карбонатной жесткости – временная. В процессе нагрева гидрокарбонаты распадаются – образуется угольная кислота, а карбонаты кальция, гидроксиды магния выпадают в виде осадка.
- Некарбонатная – обусловлена присутствием магниевых и кальциевых кислотных солей. При кипячении не устраняется (то есть является постоянной).
Общая жесткость измеряется в GH. GH показывает суммарное содержание щелочноземельных металлов в виде ионов. Для примера – в воде, значение GH которой близкое к нулю, аквариумные рыбки не живут, употреблять ее в пищевых целях также не рекомендуется.
В каких единицах измеряется жесткость
В мире для измерения показателей жесткости используются разные значения. В России Госстандарт установил следующий показатель – моль на кубический метр. Числовое значение жесткости, которое выражается в молях на кубический метр, равняется числовому значению жесткости в миллиграмм-эквивалентах на литр. На западе используют немецкий (d°, dH), французский (f°), американский (ppm CaCO3) градусы.
Как повысить и понизить жесткость воды в аквариуме. Определение временной, или карбонатной жесткости
Чтобы создать комфортные условия для жизни аквариумных рыбок, важно использовать воду оптимальной жесткости, с заданным кислотно-щелочным балансом. Чтобы повысить жесткость воды, используют известняк и мрамор. Чем мягче вода, тем быстрее она повысит жесткость. Другой способ – химический, с применением хлористого кальция и магнезии. Максимальный эффект достигается при использовании обоих препаратов одновременно.
Чтобы уменьшить жесткость, воду нужно прокипятить. Как долго это следует делать? Учтите, что для снижения жесткости вдвое, кипятить воду нужно минимум в течение получаса. Другой способ – вымораживание. Воду наливают в пластиковый контейнер и помещают в морозилку. Затем лед растапливают, а полученную воду используются в пищевых или любых других целях.
Если объемы воды большие, проще будет использовать специальное оборудование. Широкое распространение в быту в последние годы получили установки обратного осмоса. Для расчета необходимого объема водопроводной воды используйте формулу – вычитание объема воды, получаемой из водопровода, из объема с заданной жесткостью, который нужно получить.
Часто методы умягчения используют комбинированно. Например, одну часть солей жесткости убирают реагентным способом, а другую с помощью катионного обмена. Приведем формулы содово-известкового способа умягчения:
Са(НСО3)2 + Са(ОН)2 = 2СаСО3 + 2Н2О
В итоге Mg(OH)2 коагулирует, выпадая в осадок. Затем, в целях устранения некарбонатной жесткости, вводится Na2CO3. Последующие химические реакции:
Na2CO3 + CaSO4 = CaCO3 + Na2SO4 и Na2CO3 + СаС12 = СаСО3 + 2NaCl.
В итоге образуется углекислый кальций, выпадающий затем в осадок. Реагенты вводят в разные зоны:
- хлор – во всасывающие трубопроводы;
- коагулянт – в трубопровод перед смесителем либо непосредственно в смеситель;
- известь – вместе с коагулянтом;
- уголь активированный – перед фильтрами;
- хлор и аммиак – в фильтрованную воду.
Опреснение, обессоливание, удаление растворенных газов, железа, стабилизация – это специальные способы очистки. Так если для снижения жесткости используются методы катионирования или ионного обмена, речь идет об обессоливании. Вода, которая получается на выходе, не содержит ни анионов, ни катионов солей.
Как измерить жесткость
Для оценки показателей жесткости воды используются следующие способы:
- Комплексонометрическое титрование трилоном Б. Метод сложный и самый точный.
- Покупные тесты. Не на 100% точные, зато простые и недорогие.
- Измерение электропроводности. Используйте кондуктометр.
- С помощью ионометра и ионоселективных электродов.
- С применением методики титрования соляной кислотой проб воды. Сложный и не очень точный метод. То же самое можно сказать о тестах с применение хозяйственного мыла.
Под титрованием подразумевается добавление в воду реагента требуемой концентрации. Концентрация солей жесткости определяется в зависимости от реакции реагента с водой. Приготовить реактив просто – достаточно смешать кислоту с дистиллированной водой в заданных пропорциях. Готовый раствор опасности не представляет.
Проще всего использовать готовые тексты. Для этого 5 мл воды наливается в стаканчик, затем в жидкость по каплям добавляется содержимое теста, после каждой капли вода перемешивается. Делать так нужно до тех пор, пока цвет не станет зеленым вместо розового.
Влияние жесткости воды, нормативные требования и рекомендации
Какую воду можно употреблять для приготовления пищи и питья? Требования относительно жесткости жидкости зависят от условий конкретной местности. Учтите, что слишком жесткая вода имеет горький вкус и негативно влияет на работу органов пищеварения. ВОЗ конкретные цифры не называет, хотя исследований на тему связи качества воды с заболеваниями сердца, сосудов и других органов организма проводились неоднократно. Слишком мягкая вода – это тоже плохо, поскольку она нарушает водно-солевой баланс. Жидкость с жесткостью от 4 мг-экв/ чревата – главная причина образования накипи на внутренних деталях отопительных систем. Вредна она и для кожи, волос.
Вместо заключения
Жесткость – важный параметр воды, который зависит от количества и типа растворенных в ней минеральных веществ. Смягчение следует делать только после предварительного анализа. Почему? Потому что не все меды смягчения снижают содержание минеральных веществ – они могут просто превращать соли жесткости в соли, которые никак не влияют на рассматриваемый показатель.
Жесткость воды как определить в домашних условиях
Неочищенная вода из водопровода или природных источников имеет повышенную степень жесткости. Этот параметр напрямую воздействует на физико-химические и органолептические свойства жидкости. Вода с высоким содержанием солей жесткости ухудшает состояние кожи и волос, нарушает работу сальных желез, сердца, пищеварительного тракта. Она приводит к поломкам бытовой техники, оставляет следы на сантехнике, делает жестким белье после стирки. Можно предупредить эти неприятности заранее, понизив жесткость воды в домашних условиях.
Понятие и разновидности жесткости воды
Немногие знают, что такое жесткость воды и как от нее можно избавиться в домашних условиях. Под жесткостью понимают количество содержащихся в воде солей Ca и Mg. Чем выше их концентрация, тем жестче жидкость. Различают несколько видов жесткости:
- Карбонатная (временная). Зависит от содержания в воде солей угольной кислоты. При кипячении химические соединения распадаются и образуют нерастворимый осадок.
- Некарбонатная (постоянная). Обусловлена присутствием в воде солей кальция, магния, бария или стронция на основе сильных кислот. Карбонатная жесткость остается после кипячения. Ее расчет выполняют на основании солей кальция и магния, пренебрегая долей бария и стронция ввиду их малого содержания.
- Общая. Под ней понимают суммарное содержание всех солей жесткости.
Для измерения концентрации солей кальция и магния в РФ используется стандартная единица измерения - градус жесткости (°Ж). В соответствие с ГОСТ 31865-12, он численно равен содержанию ½ миллимоля Ca или Mg на 1 литр (1 °Ж = 1 мг-экв/л).
Кальций и магний участвуют во многих природных химических процессах, поэтому их соли присутствуют в естественном виде в воде из разных водоемов. По степени жесткости вода бывает:
- мягкая - не превышает 2 °Ж;
- средней жесткости - от 2 до 8 °Ж;
- жесткая - более 8 до 12 °Ж;
- очень жесткая - свыше 12 °Ж.
Обычно, даже по визуальным признакам можно узнать жесткость воды домашних условиях. В природе мягкую воду можно найти в болотистой местности, на торфяниках. Вода средней жесткости встречается в разных регионах, такие показатели обычно у воды из скважин и колодцев. Жесткая присутствует на территориях с повышенным содержанием химических солей, при наличии различных загрязнителей. Она требует тщательной очистки. Сверхжесткая вода встречается вблизи горных пещер и шахт. Без обработки ее нельзя использовать для питья.
Как определить жесткость воды в домашних условиях
Чтобы эффективно умягчить воду из водопроводной системы или другого источника, нужно правильно измерить уровень ее жесткости. Это позволит грамотно выбрать метод смягчения, корректно подобрать оборудование (если потребуется).
Для точного определения состава исходной воды нужно отправить пробы на лабораторные исследования. Но если высокая точность не требуется, можно провести измерения самостоятельно. Для этого необходимо знать, чем определить жесткость воды в домашних условиях. Рассмотрим основные способы диагностики:
- Тест-полоски. Это экспресс-метод измерить жесткость воды дома, при котором бумажная полоска с нанесенным реагентом опускается в жидкость. Соли жесткости вступают в химическую реакцию, происходит изменение цвета тестера: чем выше концентрация, тем ярче оттенок. Тест-полоски продаются в зоомагазинах, магазинах бытовой техники.
- С использованием зеркала - еще один способ проверить жесткость воды в домашних условиях. На стеклянную поверхность наносятся несколько капель воды. После полного испарения жидкости нужно проанализировать оставшийся на стекле осадок. Метод предполагает использование сырой и кипяченной воды, соответственно, для нахождения общей и временной жесткости. Чем меньше осадок, тем мягче вода.
- При помощи мыла. Повышенное содержание солей ухудшает мылкость хозяйственного мыла. Это свойство можно использовать, чтобы достаточно точно проверить жесткость воды домашних условиях. Нужно измельчить 1 г мыла и аккуратно, не взбивая пену, растворить его в небольшом объеме нагретой дистиллированной воды. Высота уровня жидкости зависит от жирности мыла: для 60% надо налить 6 см; для 72% - 7 см. При этом, в каждом сантиметре раствора будет содержаться количество мыла, достаточное для связывания всех солей жесткости в 1 л воды при их концентрации 1°dH (немецкая единица измерения). Затем в банку наливают 0,5 л исследуемой воды. Сюда же добавляется мыльный раствор и перемешиваются до образования белой пены - она свидетельствует о связывании мылом солей жесткости. Замерив уровень оставшейся жидкости, можно найти искомую жесткость. Каждый сантиметр влитого мыльного раствора свяжет в 0,5 л воды количество солей жесткости в 2 °dH. Если до образования пены пришлось влить 3 см раствора, значит жесткость составляет 6 °dН.
- По накипи на чайнике. При кипячении жесткой воды на внутренних стенках прибора появляется несмываемый плотный налет. Этот метод требует достаточно много времени - вода с содержанием солей более 10 °Ж оставит заметный слой накипи примерно за месяц.
- По разводам на сантехнике. Даже без кипячения жесткая вода приводит к появлению известковых отложений. Она забивает сетки кранов, лейку, резьбу на разъемных соединениях.
- С помощью TDS-метра. Он измеряет электропроводность воды, на основании чего высчитывается жесткость. Способ достаточно сложный, он требует наличия опыта. К тому же, на электропроводность влияет общее содержание солей в воде, а не только кальция и магния.
Также в домашних условиях можно определить жесткость по органолептическим показателям. Вода с высоким уровнем минерализации разительно отличается по вкусу от чистой. Наличие солей магния придает ей характерный горьковатый привкус. Для оценки водопроводной воды можно провести эксперимент: приобрести воду разной степени жесткости и сравнить ее по вкусу.
Бытовые способы умягчения - как понизить жесткость воды в домашних условиях
Чтобы умягчить воду собственными силами, можно использовать такие варианты:
- Отстаивание. При отстаивании воды в течение минимум 24 часов содержащиеся в ней карбонаты частично выпадают в нерастворимый осадок. Метод используется для незначительного смягчения.
- Кипячение - самый простой способ уменьшить жесткость воды в домашних условиях. Под воздействием высоких температур происходит разрушение ионных связей в соединениях, что приводит к высвобождению элементов и выпадению осадка. Способ эффективен для снижения временной жесткости.
- Замораживание. Очищаемую жидкость помещают в морозильную камеру. Чистая вода застывает первой, а остаток содержит концентрированный жесткий раствор - его сливают. Талая вода не изменяется по структуре, она подходит для приготовления пищи, полива растений.
- Обработка пищевыми (химическими) реагентами. Здесь применяются пищевая сода, кальцинированная сода, лимонная и уксусная кислота, синтетические таблетирование реагенты. Так умягчают воду в домашних условиях для бытового использования и хозяйственных нужд (стирки, мытья посуды, уборки).
- Торфование. Для снижения жесткости воды используется самодельный фильтр из завернутого в ткань торфа. Его можно использовать для нескольких циклов домашней очистки.
Промышленное и бытовое удаление солей жесткости от компании Диасел
Для глубокого умягчения используется специализированное водоочистительное оборудование:
- Фильтры умягчения - различают картриджные, реагентные, электромагнитные. Для домашнего использования наиболее востребованы кувшинные фильтры со сменными кассетами. Фильтрация является основным способом смягчения воды для бытовых нужд.
- Ионнообменные фильтры - они эффективно удаляют соли жесткости, железо. В их состав входят многокомпонентные смолы (Экотар, Экомикс) - при прохождении через них в воде происходит замена ионов кальция и магния на более нейтральные элементы.
- Обратный осмос - установки с фильтрующими мембранами для комплексной очистки и смягчения воды.
Умягчение- это обязательный этап водоподготовки, улучшающий вкусовые качества жесткой воды и делающий ее безопасной для бытовых приборов. В домашних условиях устранить жесткость можно лишь частично, для получения воды высокого качества потребуется профессиональные системы фильтрации. Купить оборудования для умягчения воды можно в нашей компании. Для правильного выбора перед оформлением заказа проконсультируйтесь с нашими менеджерами. Выберите удобный способ для связи в разделе "Контакты".
Заявка на подбор оборудования
Жесткость воды - важный показатель качества воды
Жесткость водыявляется важным показателем качества воды. Vodalab рассказывает о жесткости воды, ее видах и способах умягчения воды.
ЖЕСТКОСТЬ ВОДЫ
Жесткая вода чаще всего ассоциируется с накипью на дне чайника или ощущением мыла на руках после мытья рук, некоторые испытывают ощущение «жестких волос». По этому критерию люди обычно оценивают качество воды. В этой статье мы рассмотрим жесткость со стороны физики и химии, изучим ее свойства, разновидности, влияние на здоровье человека и способы ее устранения жесткости воды.
Вода, содержащая большое количество солей кальция
Эффект жесткой воды
Жесткость воды — это концентрация растворённых в ней солей магния (Mg) и кальция (Ca): гидрокарбонатов, хлоридов и сульфатов. Проще говоря, жесткой называется вода, содержащая в себе большое количество солей. Почему воду назвали «жесткой»? Женщины в старину стирали вещи на берегу рек и озер, в воде которых содержат кальций, отчего ткань становилась жесткой на ощупь.
Жесткость воды делится на 3 вида:
- Карбонатная, т.е. временная. Она ликвидируется с помощью обычного кипячения воды и обусловлена гидрокарбонатами кальция и магния Са(НСО3)2; Mg(НСО3)2.
- Некарбонатная, т.е. постоянная. Возникает из-за присутствия других солей, например CaSO4, Ca(Cl)2, MgSO4, Mg(Cl)2. При кипячении воды не устраняется.
- Общая. Представляет собой суммарную концентрацию ионов кальция и магния. Представляет собой сумму карбонатной и некарбонатной жесткости.
Единицы измерения жесткости:
Не существует единой единицы измерения жесткости. В России, в соответствии с Госстандартом, в качестве единицы жесткости воды установлен моль на кубический метр (моль/м3). В Германии — 2.8DH°; во Франции — 5F°; в Америке — 50.05 ppm CaCO3.
Классификация воды по жесткости:
| Характеристика | Жесткость, мг-экв/л |
| очень мягкая вода | до 1,5 мг-экв/л |
| мягкая вода | от 1,5 до 4 мг-экв/л |
| вода средней жесткости | от 4 до 8 мг-экв/л |
| жесткая вода | от 8 до 12 мг-экв/л |
| очень жесткая вода | более 12 мг-экв/л |
Согласно требованиям СанПиН 2.1.4.1074-01 жесткость питьевой воды должна быть не выше 7 мг-экв/л.
Влияние на здоровье человека:
Как же влияет жесткая вода на наш организм? Медики связывают появление мочекаменной болезни именно с этой особенностью воды. Но на данный момент официального подтверждения этой гипотезе нет. Но мы знаем, что слишком жесткая вода неблагоприятно влияет на органолептические свойства воды, придавая ей горьковатый вкус. Также жесткая вода сушит нашу кожу и волосы. Однако, полностью переходить на мягкую воду не рекомендуется. Наш организм нуждается в солях кальция и магния для укрепления сердечно-сосудистой системы. А вот комнатные растения лучше поливать мягкой или талой водой.
Способы борьбы с жесткой водой:
Для смягчения жесткости воды специалисты рекомендуют приобрести умягчители, которые являются самыми эффективными в борьбе с солями жидкости. Также существует несколько способов смягчения воды в домашних условиях, самым простым и привычным из которых является кипячение воды.
Для борьбы с постоянной жёсткостью воды используют такой метод, как вымораживание льда. Необходимо просто постепенно замораживать воду. Когда примерно 90% жидкости превратится в лед, нужно разморозить его обратно, а соли останутся в оставшейся незамороженной жидкости.
При выборе степени жесткости воды лучше придерживаться середины. Самым оптимальным является использование воды средней жесткости для приготовления пищи и мягкой воды для гигиенических процедур. А чтобы ваша бытовая техника не страдала от повышенной жесткости, лучше приобрести умягчитель.
Заказать анализ воды на жесткость вы можете на нашем сайтеvodalab. Каждый из представленных на сайте анализов содержит исследование воды на жесткость.
О других загрязнителях воды, таких как железо, мутность и марганец, вы также можете узнать подробнее в нашем блоге.
Жесткость воды
Жесткость воды
Существуют разные типы жесткости воды:
| ● TH | – | Общая жесткость | |
| ● CH | – | Карбонатная жесткость | (временная твердость) |
| ● NCH | – | Негарбонатная жесткость | (постоянная твердость) |
| ● PsH | – | Псевдотвердость |
Общая жесткость TH
Общая жесткость определяется как молярные концентрации всех мульти- -валентных катионов в воде (т.е.е. все, кроме одновалентных катионов):
| (1) | Общая жесткость TH = Σ многовалентных катионов |
На практике он часто используется как сумма двух наиболее важных пресноводных катионов, кальция и магния:
| (1а) | TH ≈ [Ca] + [Mg] |
Но это только приблизительное значение, хотя и хорошее. Правильная формула (согласно определению в 1 ):
| (1б) | TH = [Ca] + [Mg] + [Sr] + [Ba] + [Fe] + [Mn] + [Al] +… |
Существует несколько шкал жесткости воды.Например, он может быть выражен в мэкв / л (единицы СИ), или в ppm CaCO 3 , или в немецких градусах жесткости:
.| (2а) | TH, мг-экв / л | = | 2 × ([Ca в мМ] + [Mg в мМ]) |
| (2б) | TH в миллионных долях | = | 100,1 × ([Ca в мМ] + [Mg в мМ]) |
| (2c) | TH дюйм ° d | = | 0.1339 × [Ca в мг / л] + 0,2307 × [Mg в мг / л] |
Правила разговора с другими устройствами приведены в таблице ниже. Общая жесткость TH используется для классификации водных растворов по четырем категориям жесткости воды.
Примечание. Если концентрации ионов Ca и Mg выражены как «ppm CaCO 3 », 1a также отображается в виде:
| (3) | Общая жесткость TH = жесткость по кальцию + жесткость по магнию |
Карбонатная жесткость CH
В то время как общая жесткость в 1 определяется содержанием катионов , существует также противоположная точка зрения, взятая из содержания анионов , которое делит общую жесткость на карбонатную жесткость CH (временную жесткость) и некарбонатную жесткость. NCH (постоянная твердость):
| (4) | Общая жесткость TH = CH + NCH |
Карбонатная жесткость напрямую зависит от щелочности:
| (5а) | CH в мэкв / л | = | [Алк в мэкв / л] |
| (5б) | CH дюйм ° dH | = | 2.809 × [Алк в мэкв / л] |
Это означает, что в химии воды термины карбонатная жесткость и щелочность (т. Е. Щелочность M или общая щелочность) являются синонимами:
| (6) | Карбонатная жесткость CH = Щелочность |
Программа вычисляет TH и CH и отображает обе величины в таблицах результатов, как показано здесь.
Неркабонатная жесткость NCH
И общая жесткость, и щелочность (т.е.е. карбонатная жесткость) - общие параметры анализа воды. Некарбонатная жесткость - согласно 4 - разница обоих величин:
| (7) | NCH = TH - CH |
Карбонатная жесткость называется временной твердостью , потому что карбонаты Ca и Mg осаждаются в виде минералов при нагревании, тогда как Ca и Mg, связанные с сульфатами, хлоридами или нитратами, не осаждаются при нагревании (поэтому NCH называется постоянной твердостью ) .
Альтернативная интерпретация. Нкарбонатная жесткость - это мера превышения сильных кислот над сильными основаниями:
| (8) | NCH = сильные кислоты - сильные основания |
При анализе воды сильные кислоты проявляют себя в присутствии некарбонатных анионов, таких как сульфат, хлорид, нитрат. С другой стороны, сильные основания обозначены одновалентными катионами (например,грамм. Na, K, аммоний). Таким образом, 8 преобразуется в
| (9) | NCH [мэкв / л] ≈ (2 × сульфат + хлорид + нитрат) - (Na + K + аммоний) |
, где измеренные концентрации следует вводить в ммоль / л.
Псевдотвердость PsH
Три величины, TH, CH и NCH, образуют стандартный словарь жесткости воды почти во всех учебниках. Однако проблема возникает, если измеренная щелочность (т.е.е. CH) превышает общую жесткость: CH> TH. В этом частном случае 4 теряет смысл.
Для решения проблемы терминология твердости должна быть расширена на дополнительную величину - псевдотвердость PsH (или «кажущуюся твердость»). Он определяется как «отрицательный NCH» и выражается обратной цифрой 8 :
.| (10) | PsH = сильные основания - сильные кислоты = - NCH |
| (11) | PsH [мэкв / л] ≈ (Na + K + аммоний) - (2 × сульфат + хлорид + нитрат) |
Другими словами, PsH - это часть карбонатной жесткости, которая принадлежит одновалентным катионам (Na, K, аммоний).
Расширение общего отношения твердости
За счет дополнительного количества PsH мы можем расширить «уравнение стандартной твердости » (4) :
| (12) | Жесткость воды: TH + PsH = CH + NCH |
Важно отметить, что PsH и NCH являются взаимоисключающими в приведенной выше формуле: либо сильные основания перевешивают сильные кислоты (тогда NCH = 0), либо наоборот (тогда PsH = 0).Таким образом, 12 становится:
| (13а) | TH ≥ CH: | TH = CH + NCH | PsH = 0 |
| (13б) | TH | TH + PsH = CH | NCH = 0 | |
, где 13a представляет собой «стандартное» соотношение твердости обычных учебников.
Пример: TH ≥ CH
Случай TH ≥ CH характерен почти для всех природных вод.Для иллюстрации возьмем в качестве примера воду C1.sol (кнопка Открыть ) со следующими параметрами:
| т | 10 ° С |
| pH | 7,34 |
| Алк | 2,50 мМ |
| Ca | 1,40 мм |
| мг | 0,23 мМ |
| Na | 0,30 мМ |
| К | 0.05 мм |
| Класс | 0,25 мМ |
| SO4 | 0,38 мМ |
| NO3 | 0,15 мМ |
Запустите пробу воды, нажав кнопку Старт . Программа жалуется на ненулевой CBE, и мы устанавливаем точный баланс заряда, регулируя DIC (который снижает щелочность с 2,50 до 2,45 мэкв / л). Полученные значения твердости (как показано в столбце таблицы Output1 ):
| TH = 2.45 мэкв / л |
| CH = 3,26 мэкв / л |
Из разницы получаем: NCH = 0,81 мэкв / л. Псевдотвердости нет (PsH = 0). Общая жесткость определяется суммой Ca и Mg: TH = (2 × 1,40 + 2 × 0,23) мэкв / л = 3,26 мэкв / л - как показано на диаграмме выше.
Пример: TH
Мы используем тот же самый пример воды C1.sol и добавляем 2 мМ NaOH (с кнопкой Reac ) .
За счет добавления 2 мэкв / л сильного основания щелочность и, следовательно, CH увеличиваются на 2 мэкв / л , при этом общая жесткость остается неизменной:
| CH = 4,45 мэкв / л |
| TH = 3,26 мэкв / л |
Здесь разница выражена псевдотвердостью: PsH = 1,19 мэкв / л. Нет НЧ.
Значение PsH также можно рассчитать, подставив молярные концентрации входящей воды в 11 :
| (14) | PsH = (2.30 + 0,05) - (2 × 0,38 + 0,25 + 0,15) = 1,19 мэкв / л |
Обратите внимание, что Na также включает добавку 2 мМ NaOH : Na = (2,0 + 0,3) мэкв / л . Расчетное значение 14 явно показано как «Diff» на приведенной выше диаграмме.
Кальцитовые осадки. Из-за добавления 2 мМ NaOH вода становится перенасыщенной кальцитом. На нижнем графике показаны результаты при осаждении 1,37 мМ кальцита (столбец таблицы Выход2 ):
| Канал | = | (4.45 - 2 × 1,37) мэкв / л | = | 1,71 мэкв / л |
| TH | = | (3,26 - 2 × 1,37) мэкв / л | = | 0,52 мэкв / л |
| PsH | = | CH - TH | = | 1,19 мг-экв / л (без изменений) |
Другие примеры
Далее мы добавляем один или два реагента в количестве 1 мМ в чистую воду (H 2 O). Результаты около 20 расчетов приведены в таблице ниже; каждая строка относится к одному вычислению. Значения TH, CH, NCH и PsH приведены в последних столбцах.
Примечание. В случаях, когда CaCO 3 (кальцит) становится перенасыщенным (SI> 0), добавляется дополнительная строка, чтобы показать результаты после осаждения кальцита.
Таблица преобразования
Жесткость воды выражается в разных единицах:
| (15а) | Немецкий язык: | 1 ° д | = | 10 мг / л CaO |
| (15б) | Французский градус: | 1 ° f | = | 10 мг / л CaCO 3 |
| (15c) | Степени английского: | 1 ° в. Д. | = | 10 мг CaCO 3 в 0.7 л |
| (15д) | 1 часть на миллион CaCO 3 (нормы США): | 1 ° а | = | 1 мг / л CaCO 3 |
Эти единицы связаны между собой простыми правилами преобразования:
| частей на миллион CaCO 3 | ° d | ° F | ° в.д. | мэкв / л | ммоль / л | |
| 1 часть на миллион CaCO 3 | 1 | 0.06 | 0,10 | 0,07 | 0,02 | 0,01 |
| 1 ° d | 17,8 | 1 | 1,78 | 1,25 | 0,357 | 0,178 |
| 1 ° | 10,0 | 0,56 | 1 | 0,70 | 0,2 | 0,1 |
| 1 ° в. Д. | 14.3 | 0,80 | 1,43 | 1 | 0,285 | 0,142 |
| 1 мэкв / л | 50,04 | 2,8 | 5 | 3,51 | 1 | 0,5 |
| 1 ммоль / л | 100.09 | 5,6 | 10 | 7,02 | 2 | 1 |
Коэффициенты пересчета в этой таблице вытекают непосредственно из молярных масс карбоната кальция и оксида кальция:
| (16a) | CaCO 3 : | 100.09 г / моль | или | 1 мг / л CaCO 3 | = | 0,010 мМ |
| (16б) | CaO: | 56,08 г / моль | или | 10 мг / л CaO | = | 0,178 мМ |
Примечания и сноски
[последнее изменение: 2018-12-02]
.
Насколько жестка моя вода?
Проверьте свой почтовый индекс и посмотрите, живете ли вы в районе с жесткой водой, с помощью нашей карты жесткости воды. Многие люди живут в районах с жесткой водой, узнайте: насколько жесткая моя вода?
проверьте свой почтовый индекс
Что такое жесткая вода
Жесткая вода содержит большое количество растворенных минералов, в основном магния и кальция. Вода от природы мягкая, когда падает с неба, и становится жесткой после контакта с землей.
Если дождевая вода попадает в область с пористыми породами, такими как известняк, вода проникает в землю и по мере прохождения собирает и растворяет частицы и минералы, такие как кальций и магний, приобретая твердость. Если вода падает на непористый камень, такой как гранит, вода не может проникнуть в землю и, следовательно, не может собирать частицы или минералы, и поэтому остается мягкой.
Уровень жесткости воды на юго-востоке Англии и в Лондоне преимущественно высок. В Шотландии, Ирландии и Уэльсе вода в основном мягкая, как вы можете видеть на карте жесткости воды.
Как измеряется жесткая вода?
Жесткая вода измеряется в частях на миллион (PPM), и количество частиц жесткости, растворенных в воде на миллион частиц, дает оценку. Этот рейтинг развивался с течением времени до следующих категорий:
| частей на миллион | Жесткость воды |
|---|---|
| 0-50 частей на миллион | Мягкая. |
| 51 - 100 мм в минуту | В меру мягкая. |
| 101 - 150 мм в минуту | Немного жестко. |
| 151 - 200 частей в минуту | Умеренно твердый. |
| 201 - 275 частей на миллион | Трудно. |
| 276 - 350 частей на миллион | Очень сложно. |
| 350 + PPM | Агрессивно твердый. |
Проблемы, связанные с жесткой водой
Когда жесткая вода попадает из водопровода в наши дома для приготовления пищи, уборки, стирки и обогрева, могут возникнуть проблемы. Миллионы людей в Великобритании получают жесткую воду из водопровода, причем в Лондоне есть особенно большие районы с жесткой водой.Когда молекулы жесткой воды перемешиваются (нагреваются) в чайниках, посудомоечных машинах и других бытовых приборах, жесткость может выпадать в виде накипи.
Накипь- это не то, что вам нужно в вашем доме по многим причинам, включая блокировку и повреждение труб, снижение эффективности или торможение бытовых приборов, включая бойлер.
Распространенные проблемы с жесткой водой и известковыми отложениями:
- Запорные клапаны
- Переходник в трубопроводе
- Менее эффективные приборы
- Рост счетов за электроэнергию и газ
- Накипь (см. Изображение)
- Более длительное время очистки
- Неисправность котла
- Плохой внешний вид поверхности (хромирование)
Что такое смягчитель воды?
Система смягчения воды подключается непосредственно к водопроводу и работает, пропуская воду через систему, удаляя частицы жесткой воды из воды перед тем, как выпустить умягченную воду обратно в систему водоснабжения.Умягчители воды Aqua Cure бывают разных размеров для домашнего использования, чтобы поместиться под кухонную раковину или шкаф, и более крупных размеров для больших домашних хозяйств и коммерческого использования.
Бит химии:
Жесткая вода проходит через цилиндр внутри устройства для смягчения воды, содержащий гранулы ионообменной смолы, заполненные ионами натрия (Na). Минералы жесткой воды, такие как магний (Mg) и кальций (Ca), вступают в реакцию со смолой и обмениваются местами с ионами натрия (Na), оставляя исходящую воду с ионами натрия вместо жесткой воды, вызывая минералы.
Каждый умягчитель может смягчить определенное количество воды до достижения максимальной емкости и больше не имеет ионов натрия для обмена. После достижения максимальной литровой емкости (каждый умягчитель отличается) ионообменную смолу промывается соленым солевым раствором, регенерируя ионы натрия (Na) и удаляя минералы жесткости, такие как магний (Mg) и кальций (Ca). Теперь процесс сброшен и снова готов к запуску процесса обмена с входящей питательной водой.
Виды смягчителей воды:
Измеренная регенерация:
Дозированная регенерация происходит после того, как через смолу прошло заданное количество воды. Все наши умягчители воды с дозатором предварительно настраиваются во время производства для простоты использования и экономии времени при первоначальной настройке. Преимущество дозированного умягчителя воды заключается в том, что он будет регенерироваться при достижении полной загрузки.
Регенерация по времени:
Альтернатива дозированной системе умягчения воды, которая программируется при первоначальной настройке.По истечении заданного времени регенерации устройство для смягчения воды регенерируется автоматически. Проблема с этим методом заключается в том, что в смоле все еще может оставаться достаточно ионов натрия для продолжения умягчения воды, но таймер установлен на раннюю регенерацию, это может привести к потере соли, и здесь, в Aqua Cure, мы выбрали дозированную регенерацию умягчителей воды. .
Какие существуют варианты емкости?
Выбор кондиционера подходящего размера зависит от ряда вещей. Чтобы упростить задачу, мы разделили наш ассортимент бытовых кондиционеров на следующие категории в зависимости от того, сколько человек живет в доме.
Обслуживание и установка:
Техническое обслуживание:
Во все смягчители воды необходимо добавлять соль для смягчения воды, так как в ней содержатся ионы натрия (Na), необходимые для создания рассола, который омывает и регенерирует смолу. Типы соли различаются в зависимости от вашей системы умягчителя. Наши системы требуют соли в таблетках для обновления смолы.
Превосходная производительность достигается за счет более дорогой, тонкой и более эффективной смолы, содержащейся в емкостях большой емкости, что приводит к более умягченной воде на каждый килограмм используемой соли.Для смягчителя воды требуется доступ к электрической розетке, что также означает, что замена батарей не требуется. Все функции машины выполняются автоматически с помощью предварительно настроенного сложного клапана с регулируемым дозированием.
Установка
Все наши устройства для смягчения воды поставляются со всем необходимым, чтобы установить устройство для смягчения воды и сразу начать пользоваться умягченной водой, включая бесплатный мешок соли. Все наши умягчители предварительно упакованы со всеми шлангами и установочными компонентами, необходимыми для установки на 15-миллиметровую трубу (стандарт Великобритании), включая:
- Шланги и соединители
- Сливной шланг
- Юбилейный клип
- Соль для смягчения воды
15 мм Установочный комплект:
- 2 компрессионных тройника - 15 мм с наружной резьбой 3/4 дюйма
- Обратный клапан
- Компрессионный Ballofix 15 мм
- Тройник компрессионный, равномерный 15мм
Гарантия:
На все наши водоумягчители с дозатором предоставляется 24-месячная гарантия и сервисная карта, которую можно заполнить и отправить нашим партнерам по обслуживанию.Вы получите 24-месячную гарантию производителя на детали и работу со дня покупки.
Бесплатная доставка:
Мы предлагаем бесплатную доставку всего ассортимента водоумягчителей с дозатором при заказе на материковую часть Великобритании.
.Жесткость воды - MEL Chemistry
Реагенты
Безопасность
- Наденьте защитные перчатки и очки.
- Проведите эксперимент на лотке.
- Поставьте плиту на пробковую подставку для горячих горшков. Не трогайте плиту после эксперимента - дождитесь, пока она остынет.
- Перед зажиганием свечи снимите защитные перчатки.
Общие правила безопасности
- Не допускайте попадания химикатов в глаза или рот.
- Не подпускайте маленьких детей, животных и лиц без защитных очков к экспериментальной зоне.
- Храните этот экспериментальный набор в недоступном для детей младше 12 лет.
- После использования очистите все оборудование.
- Убедитесь, что все контейнеры полностью закрыты и правильно хранятся после использования.
- Убедитесь, что все пустые контейнеры утилизированы надлежащим образом.
- Не используйте оборудование, которое не входит в комплект поставки или не рекомендовано в инструкции по эксплуатации.
- Не заменяйте продукты в оригинальной упаковке.Немедленно утилизируйте.
Общая информация по оказанию первой помощи
- В случае попадания в глаза: промыть глаза большим количеством воды, при необходимости держать глаз открытым. Немедленно обратитесь за медицинской помощью.
- При проглатывании: прополоскать рот водой, выпить свежей воды. Не вызывает рвоту. Немедленно обратитесь за медицинской помощью.
- В случае вдыхания: вывести человека на свежий воздух.
- В случае контакта с кожей и ожогов: промыть пораженный участок большим количеством воды в течение не менее 10 минут.
- В случае сомнений немедленно обратитесь за медицинской помощью. Возьмите химическое вещество и контейнер с собой.
- В случае травмы всегда обращайтесь к врачу.
Консультации для взрослых
- Неправильное использование химикатов может привести к травмам и ущербу для здоровья.Выполняйте только те эксперименты, которые указаны в инструкции.
- Этот экспериментальный набор предназначен только для детей старше 12 лет.
- Поскольку способности детей очень сильно различаются, даже в пределах возрастных групп, взрослые должны проявлять осмотрительность при выборе экспериментов, подходящих и безопасных для них. Инструкции должны позволять руководителям оценивать любой эксперимент, чтобы установить его пригодность для конкретного ребенка.
- Наблюдающий взрослый должен обсудить предупреждения и информацию о безопасности с ребенком или детьми до начала экспериментов. Особое внимание следует уделять безопасному обращению с кислотами, щелочами и легковоспламеняющимися жидкостями.
- В зоне, окружающей эксперимент, не должно быть никаких препятствий и места для хранения продуктов. Он должен быть хорошо освещен и вентилирован и находиться рядом с водопроводом.Должен быть предусмотрен прочный стол с термостойкой столешницей.
- Вещества в неповторяемой упаковке должны быть израсходованы (полностью) в течение одного эксперимента, то есть после открытия упаковки.
Часто задаваемые вопросы и устранение неисправностей
Раствор в колбе не мутнеет после шага 6.
Возможно, раствор в колбе еще недостаточно нагрелся.Подождите 5 мин. дольше.
Как пользоваться термостикером?
Наклейте наклейку на колбу или плиту. При температуре около 60–70 o С треугольник меняет цвет с черного на желтый, чтобы предупредить о том, что объект, к которому он прикреплен, горячий и к нему нельзя прикасаться! Вы можете брать колбу или дотрагиваться до нее, только когда она остынет и треугольник снова станет черным.
Другие эксперименты
Пошаговая инструкция
- Налейте воду в колбу до отметки «40».
- Добавьте туда весь 0,2 М раствор хлорида кальция CaCl 2 из флакона.
- Возьмите топливную плиту и поставьте на нее свечу. Снимите защитные перчатки и зажгите свечу. Установите диффузор пламени на плиту, как показано.
- Установите колбу на диффузор пламени. Подождите 15 мин.
- Вылейте весь 0,3 М раствор гидрокарбоната натрия NaHCO 3 из флакона.
- Вода в колбе станет мутной.
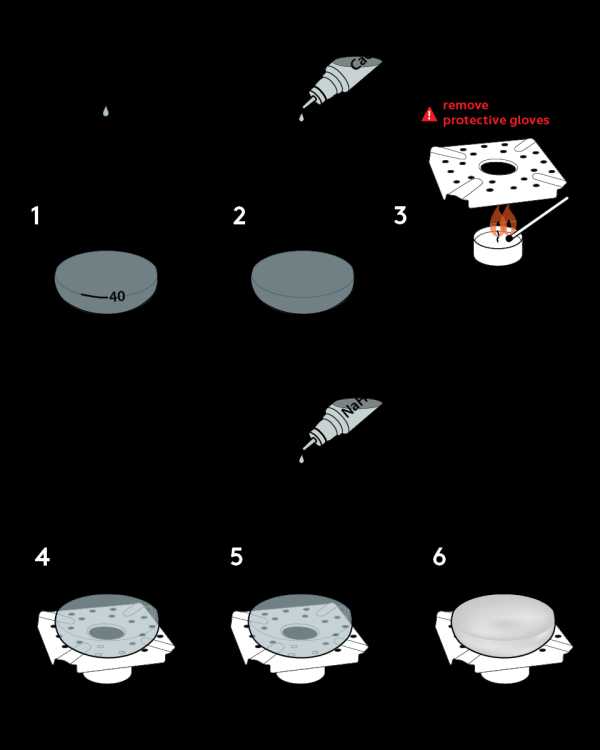
Утилизация
Утилизировать твердые отходы вместе с бытовым мусором.Вылейте растворы в раковину. Смыть большим количеством воды.
Научное описание
Что такое жесткость воды?
Жесткость воды - это величина, отражающая количество растворенных в воде солей кальция, магния и железа. Есть временная твердость (которую можно удалить) и постоянная твердость. Временная твердость обусловлена бикарбонатами кальция и магния (Ca (HCO 3 ) 2 и Mg (HCO 3 ) 2 ), а постоянная жгут - их сульфатами ((CaSO 4 и MgSO 4 ) и хлориды (CaCl 2 и MgCl 2 ).
Таким образом, жесткая вода - это вода, которая одновременно содержит много солей кальция, магния и железа.
Почему мы добавляем СаCl 2 ?
Добавляя в воду хлорид кальция CaCl 2 , мы искусственно увеличиваем ее жесткость. Как упоминалось выше, CaCl 2 вызывает постоянную (то есть не устраняемую кипячением) жесткость воды. И первая часть эксперимента продемонстрировала этот факт: при кипячении на стенах не происходит заметных осадков.
Что происходит, когда мы добавляем NaHCO 3 ?
Добавление бикарбоната натрия NaHCO 3 дает образование бикарбоната кальция в растворе:
2NaHCO 3 + СаCl 2 ↔ Ca (HCO 3 ) 2 + 2NaCl
А из-за образования Ca (HCO 3 ) 2 жесткость нашей воды становится временной - теперь ее можно удалить кипячением.
Что происходит при нагреве воды?
Когда мы нагреваем воду, достаточно растворимый бикарбонат кальция превращается в плохо растворимый карбонат:
Ca (HCO 3 ) 2 → CaCO 3 ↓ + CO 2 ↑ + H 2 O
Белый налет на дне и стенках колбы - это карбонат кальция.
Почему образуется накипь и как ее удалить?
Накипь (или известковый налет) представляет собой нерастворимый карбонат кальция CaCO 3 , который выпал в осадок при термическом разложении бикарбоната кальция Ca (HCO 3 ) 2 :
Ca (HCO 3 ) 2 → CaCO 3 ↓ + CO 2 ↑ + H 2 O
Хотя толстый серый слой накипи не делает посуду красивее, он не приносит вреда. Кроме того, он может удалить излишнюю жесткость водопроводной воды.Кроме того, накипь легко удаляется с чайников и кастрюль, промывая их лимонной кислотой С 6 H 8 O 7 раствор:
3CaCO 3 + 2С 6 H 8 O 7 → Ca 3 (C 6 H 5 O 7 ) 2 + 3CO 2 + 3H 2 O
В результате реакции образуется цитрат кальция Ca 3 (C 6 H 5 O 7 ) 2 , который хорошо растворяется в воде.
Учить больше
Грязно-бежевый цвет окалины обусловлен присутствием оксида железа Fe 2 O 3 . Водопроводная вода содержит некоторое количество железа в виде ионов Fe 2+ , но при кипячении оно выпадает в осадок.
Интересно, что по химическому составу накипь имеет тот же химический состав, что и природный известковый налет. Иногда они находят целые горы, образованные из этого минерала. Обычно в таких массивных природных образованиях есть многочисленные пещеры - излюбленные спелеологами! Эти пещеры легко образуются в известняке: даже слабокислая природная вода на своем пути растворяет карбонаты, образуя любопытные ходы в минерале.
Кроме того, карбонат кальция является основным компонентом обычного мела, который используется для письма на доске или рисования на асфальте. Кроме того, мел используется в качестве пищевой добавки - белого пищевого красителя Е170.
Напомним, что карбонат кальция - это вещество, придающее яичной скорлупе твердость. В наборе MEL Chemistry есть эксперимент «Химия пищи», в котором карбонат кальция растворяется обычным уксусом (см. Эксперимент «Резиновое яйцо»).
Как смягчить воду?
Вода с низким содержанием солей кальция и магния называется мягкой.А процесс снятия жесткости с воды смягчается.
Самый простой способ смягчить воду, как показывает наш эксперимент, - это кипячение. При нагревании бикарбонаты кальция и магния (Ca (HCO 3 ) 2 и Mg (HCO 3 ) 2 ) подвергаются термическому разложению:
Ca (HCO 3 ) 2 → CaCO 3 ↓ + CO 2 ↑ + H 2 O
Mg (HCO 3 ) 2 → MgCO 3 + CO 2 ↑ + H 2 O
MgCO 3 + H 2 O → Mg (OH) 2 ↓ + CO 2 ↑
Кипячение (термическое умягчение) - древнейший способ умягчения воды для хозяйственных нужд.Конечно, этот процесс снимает лишь временную (карбонатную) жесткость. Постоянная жесткость сохраняется, как мы можем наблюдать в первой части нашего эксперимента: вода, насыщенная хлоридом кальция CaCl 2 , не оставляет осадка при кипячении.
Дистилляция тесно связана с кипячением. Следовательно, во время перегонки испарившаяся жидкость конденсируется на охлаждаемой поверхности и, таким образом, собирается в виде капель. Вода, очищенная таким способом, называется дистиллированной водой и не содержит ионов металлов.Дистиллированная вода из-за низкой минерализации непригодна для питья, так как она «вымывает» минералы из организма. Однако дистиллированная вода широко используется в науке и промышленности.
Ниже вы можете найти дополнительную информацию о современных методах смягчения воды.
Учить больше
Очевидно, что кипячение - один из самых простых способов смягчить воду. Однако у такого процесса есть существенные недостатки, а именно низкая эффективность и высокое потребление энергии.
Другой способ смягчить воду - использовать реагенты. Они переводят ионы магния и кальция в нерастворимую форму, добавляя определенные химические вещества - например, гидроксид кальция Ca (OH) 2 (процесс называется размягчением извести):
Ca (OH) 2 + Ca (HCO 3 ) 2 → 2CaCO 3 ↓ + 2H 2 O
Mg (HCO 3 ) 2 + 2Ca (OH) 2 → Mg (OH) 2 ↓ + 2CaCO 3 + 2H 2 O
Смягчение извести, как и кипячение, устраняет только карбонатную жесткость.Для устранения постоянной (некарбонатной) жесткости необходимо более глубокое умягчение воды, поэтому в дополнение к гашеной извести используют карбонат натрия Na 2 CO 3 :
Ca 2+ + Na 2 CO 3 → CaCO 3 ↓ + 2Na +
Mg 2+ + Na 2 CO 3 → MgCO 3 ↓ + 2Na +
MgCO 3 + Ca (OH) 2 → Mg (OH) 2 ↓ + CaCO 3 ↓
Для еще более эффективного удаления ионов кальция и магния из воды используют «большие пушки» - фосфат натрия Na 3 PO 4 :
3Ca 2+ + 2Na 3 PO 4 → Ca 3 (PO 4 ) 2 ↓ + 6Na +
3Mg 2+ + 2Na 3 PO 4 → Mg 3 (PO 4 ) 2 ↓ + 6Na +
Недостатком этого метода умягчения воды является необходимость очень точного дозирования реагентов.
В промышленности наиболее широко используется метод умягчения воды с ионообменными смолами . Вода проходит через специальный фильтр, задерживающий ионы кальция Ca 2+ , магния Mg 2+ , железа Fe 2+ и марганца Mn 2+ . Эти «пойманные» ионы заменяются ионами калия K + , натрия Na + или водорода H + , выделяемыми в раствор.
Этот метод очень эффективен для смягчения воды.Достоинства этой методики - низкая стоимость реагентов и отсутствие сложных процедур, таких как осаждение и удаление осадка. Кстати, именно так умягчают воду в посудомоечной машине. Чтобы фильтр прослужил дольше, в посудомоечную машину наливают соль NaCl, которая замещает кальций и магний и насыщает фильтр ионами натрия.
В лаборатории часто используют другой процесс очистки воды, называемый обратным осмосом. Кроме того, этот метод иногда используют даже в домашних условиях.Вода проходит через мембрану, не пропускающую соли металлов. Важно отметить, что обратный осмос может принимать только воду, которая уже была предварительно обработана. Мембрана очень тонкая и нежная: она может быть повреждена высокими концентрациями солей. Обратный осмос - очень дорогой процесс очистки воды, но, в свою очередь, относительно быстрый и удобный.
Вот это интересно!
Какая вода лучше для вас: жесткая или мягкая?
Ответ прост: все хорошо в меру.Идеальным вариантом для повседневного домашнего использования является вода средней жесткости, содержащая некоторое количество солей кальция, магния, железа и марганца. Правильный баланс - всегда путь к гармонии.
Жесткая вода
Прежде всего, давайте выясним, почему возникает проблема, когда вода слишком жесткая. Регулярное употребление жесткой водопроводной воды может способствовать образованию камней в почках и мочевом пузыре. Нет никаких других доказанных с медицинской точки зрения потенциальных опасностей для здоровья человека от его употребления. Использование жесткой воды для купания или мытья лица может часто вызывать раздражение кожи, особенно у детей.Кроме того, жесткая вода может создавать неудобства в быту: соли кальция и магния, ответственные за жесткость воды, могут образовывать нерастворимые соединения с жирными кислотами, содержащимися в мыле. Это не только увеличивает расход мыла - в некоторых регионах из-за жесткости воды на умягчение воды уходит до 35% мыла, а затем только 65% - на гигиенические нужды. К сожалению, это также приводит к осаждению нерастворимых солей кальция и магния (стеаратов) в канализационных трубах, таким образом оседая там мыльную пену.Сегодня большинство моющих средств, в отличие от обычного мыла, содержат синтетические добавки, не вступающие в реакцию с солями жесткости. Таким образом, в настоящее время уходит «мыльная проблема» жесткой воды. К сожалению, возникла другая проблема: в жесткой воде нагревательные элементы стиральных и посудомоечных машин постепенно откладывают слой накипи и в конечном итоге перестают работать из-за этого. В домашнем хозяйстве жесткая вода доставляет некоторые неудобства, но в промышленных масштабах может создать настоящие неприятности. Даже слой известкового налета толщиной в миллиметр, осевший на внутренней части оборудования, резко снижает его эффективность теплообмена.Это не только увеличивает потребление электроэнергии для самого процесса, но также может повредить оборудование. Представьте себе огромный чайник, на дне которого постоянно образуется толстый слой известкового налета. Рано или поздно он выйдет из строя! А в промышленности они используют устройства и инструменты гораздо более сложные, чем чайник. Таким образом, как системы отопления, так и системы охлаждения требуют тщательного учета подаваемой воды.
Процессы с использованием химикатов также требуют тщательной очистки воды. Например, окрашивание текстиля возможно только с использованием особо мягкой воды, потому что некоторые красители могут образовывать нерастворимые соединения с ионами кальция, магния, марганца и железа.В жесткой воде этот процесс с некоторыми красителями может быть очень сложным.
Мягкая вода
Теперь рассмотрим преимущества и недостатки использования мягкой воды.
Регулярное употребление мягкой воды может вызвать проблемы с зубами и костями, так как с питьевой водой мы обычно получаем значительное количество необходимых минералов. К счастью, проблема не такая уж большая, поскольку потребность в кальции, магнии и марганце может быть удовлетворена с помощью здорового питания.
В мягкой воде мыло пенится намного эффективнее, чем в жесткой воде. Однако для смывания моющего средства требуется значительно более мягкая вода, чем для смывания жесткой воды.
Кроме того, водопровод страдает от сверхмягкой воды: при нагревании вода с низкой концентрацией солей может постепенно растворять металлические конструкции. В химической промышленности часто используют не просто умягченную воду, а дистиллированную. Не только дистиллированная вода очень мягкая, но и не содержит многочисленных примесей, которые совершенно не влияют на жесткость воды, таких как сульфаты (SO 4 ) 2- , хлориды Cl - и натрий Na + . и ионы калия K + .
Дистиллированная вода: мягче не бывает
Дистиллированная вода - это вода, очищенная с помощью сложного процесса, называемого дистилляцией. Дистиллированная вода практически не содержит примесей. Интересно, что дистиллированная вода может быть переохлаждена ниже точки замерзания или перегрета выше точки кипения! Дистиллированная вода обычно используется в химических лабораториях и в химической промышленности, где чистота приготовленных растворов очень важна. Кроме того, дистиллированная вода используется в пищевой промышленности (для приготовления некоторых напитков), в автомобильной промышленности (для приготовления электролита для аккумуляторов), в медицине и цветной печати.
Есть также вода, дважды очищенная дистилляцией - так называемая бидистиллированная вода. По составу она очень близка к химически чистой воде. Есть ли способ получить воду еще большей чистоты? Для получения такой воды необходимо использовать гамма-излучение с последующим барботированием инертным газом - аргоном Ar.
Действительно, обычная вода содержит множество невидимых глазу примесей: соли, частицы пыли, минералы и органические соединения. Полная противоположность обычной воде - это химически чистая вода, которая содержит только молекул воды H 2 O.
.Калькулятор жесткости воды - Расчет высокой точности
- Цель использования
- Оценить спецификации RO система с реминерализацией.
- Комментарий / запрос
- Пожалуйста, также добавьте другие минералы, такие как Na +, K + и расчет щелочности / pH.
Спасибо!
[1] 2020/03/10 02:49 Мужчина / 40-летний уровень / Учитель / Исследователь / Очень /
- Цель использования
- Попытка понять, как рассчитывается твердость для Курс экологической инженерии
[2] 2019/10/11 02:43 Мужской / 20-летний уровень / Старшая школа / Университет / аспирант / Немного /
- Цель использования
- Сделать раствор
[3] 2019/07/15 11:16 Мужской / 20-летний уровень / Начальная школа / Младший школьник / Очень /
- Цель использования
- Расчет жесткости воды в помощь гражданину
[ 4] 2019/01/07 23:13 Мужской / 50-летний уровень / Другое / Очень /
- Цель использования
- Установка смягчителя воды....
[5] 2018/10/12 11: 01 Мужчина / 50 лет / Средняя школа / Университет / Аспирант / Полезно /
- Цель использования
- Разработка процесса
[6] 2018/06/16 02:25 Мужчина / 60 лет и старше / Инженер / Очень /
- Цель использования
- Для расчета жесткости колодезной воды на ферме на основе анализа минералов, проведенного на воде, чтобы помочь в определении потребностей в буферных растворах для гербицидов.
[7] 2017/03/02 05:40 Женский / 50-летний уровень / Другое / Очень /
- Цель использования
- Мг (мг / л) x4.118
- Комментарий / Запрос
- 4.118 означает
[8] 2017/03/01 18:27 Мужчины / Уровень 40 лет / Самостоятельно занятые / Очень /
- Цель использования
- очень помогите мне решение для жесткой воды. Много полезного ... много благодати
- Комментарий / запрос
- должен решить для обеспечения соответствия, если какое-либо использование является хорошим. Для решения проблемы потребуется много работы. Требуется в нормалях, а не массах
[9] 2017/02/01 05:31 - / 60 лет и старше / Инженер / Очень /
- Цель использования
- Быстрый расчет твердости.Работаю в очистке воды
[10] 24.05.2016 16:47 Мужчина / Уровень 20 / Инженер / Полезно /
Как проверить жесткость воды
Раз и навсегда разобраться в своих водных бедах
После того, как вы заметили признаки жесткой воды в доме, естественно, что вы хотите определить следующие шаги для решения проблемы - и быстро. Напоминаем, что жесткая вода обычно выглядит следующим образом:
- Пятнистая, пленчатая посуда
- Мыло, которое не пенится
- Подонки, трудно поддающиеся чистке ванны и душевые
- Сухая, скрипучая кожа
- Белая корка вокруг смесителей, водостоков и лейки
Первым шагом к решению проблем с жесткой водой является проведение теста на жесткость воды, чтобы вы могли найти лучший раствор для смягчения воды.Вот несколько способов начать работу:
Уточняйте у своего города
Каждый год до 1 июля вы должны получать краткий отчет об уверенности потребителей или отчет о качестве питьевой воды по почте или онлайн-уведомление от поставщика воды. В отчете указано, откуда берется ваша вода и что в ней, а в некоторых отчетах указывается жесткость воды. Если у вас нет, вы можете позвонить в местный водоканал, и они смогут вам сказать.
Быстрое тестирование в домашних условиях
Один из самых простых вариантов теста жесткой воды - это чистая, пустая бутылка с крышкой, чистое жидкое мыло и вода прямо из бутылки. ваш кран.Наполните бутылку на одну треть, добавьте несколько капель чистого жидкого мыла и энергично встряхните в течение нескольких секунд. Если явно не хватает пушистых пузырьков, а вода кажется мутной и / или молочной, ваша вода жесткая. В мягкой воде будет много пузырьков, а оставшаяся вода на дне бутылки будет прозрачной. Имейте в виду, что, поскольку в состав большинства мыла входят моющие средства, они пенится независимо от типа воды. Для достижения наилучших результатов используйте простое мыло, такое как Castile, без красителей, отдушек и моющих средств.
Расширенные методы тестирования
Тест бутылки с водой может хорошо работать в качестве базовой оценки, но это не самый точный способ определения уровня жесткости воды. Для этого требуется более сложный тест на жесткость воды. В набор для жесткой воды входят тест-полоски и таблица цветов. Вы можете приобрести набор для тестирования в магазине товаров для дома за 5–10 долларов или запросить у нас бесплатную тест-полоску для воды.
Наполнив стакан холодной водой из раковины для ванной комнаты , вставьте тест-полоску на несколько секунд, а затем извлеките ее.Также важно отметить, что не следует просто обмакивать полоску под проточную воду, поскольку это может привести к неточным результатам. По мере того как полоска меняет цвет, сравните ее с таблицей цветов, входящей в комплект. Каждый цвет на диаграмме соответствует жесткости вашей воды, а результаты измеряются в зернах на галлон (gpg).
Крупные магазины товаров для дома и многие интернет-магазины продают дополнительные тест-наборы, которые могут обеспечить более полную оценку воды. Они не только проверяют на жесткость, они также проверяют щелочность, хлор, железо, нитраты и / или pH.Чтобы получить наиболее тщательный анализ воды, вы можете отправить образец в стороннюю лабораторию, которая может проверить наличие специальных загрязнителей, таких как тяжелые металлы и бактерии. Обычно в этом нет необходимости, потому что домашний комплект предоставляет мгновенную информацию и результаты для большинства проблем с водой. В целом, знание своего профиля воды может помочь вам выбрать подходящее решение для любой проблемы с водой.
Какой у вас номер?
Поскольку более 85% всех домохозяйств в той или иной степени сталкиваются с жесткой водой, знание вашего «числа» позволит вам увидеть, где складывается ваша жесткость.После того, как вы проверили воду с помощью полоски или набора, следующим шагом будет использование вашего «числа», чтобы узнать, насколько жесткая ваша вода. Средняя твердость в США составляет около 13 зерен, что считается «очень твердым». Все, что превышает 14 зерен, считается «чрезвычайно трудным». Даже если вы не живете в зонах с высокой жесткостью воды, семья начинает замечать воздействие жесткой воды с жесткостью около 7 грамм. Если вы знаете свое число жесткости, с помощью этого пошагового инструмента легко найти подходящий кондиционер для дома.

 Категории
Категории Корзина
Корзина Информация
Информация Хиты продаж
Хиты продаж